-
)杂质以降低潜在致癌风险指导原则(M7)进行研究,并确定检查项目。 无机杂质参照ICH元素杂质指导原则(Q3D)进行研究,并确定检查项目。 a 取限度低者 报告阈值(reporting threshold):超出此阈值的杂质均应在检测
2022-03-25
来源: 2020年版中国药典
-
物质项下。进样体积20μl系统适用性要求理论板数按吲哚美辛峰计算应不低于2000,吲哚美辛峰与相邻杂质峰之间的分离度应符合要求。测定法精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算每片的含量,求出平均含量。
-
第5版(1974年)、第6版(1981年)、第7版(1986年)。
三、化学试剂等级
按照国家标准,根据试剂中所含杂质的多少,划分为四个等级:
一级优级纯GR绿精密分析实验;
二级分析纯AR红一般分析实验;
三级化学纯
-
进行单链切割。Alt-R® Cas9
H840A切口酶,HNH结构域失活,对非靶向链单链切割。以10μg/μL的溶液提供。100μg Cas9切口酶=610pmol。 7、Alt-R® dCas9蛋白:S.
pyogene来源Cas
-
4. CRISPR-Cas9多重靶向编辑多个基因。实验组(1-4泳道)为Cas9表达克隆及分别表达靶向p53, HUWE1, NCL3 和
GFP基因的sgRNA克隆质粒共转染HEK293t
GFP稳转细胞。对照组(5-8泳道)为
-
不适宜人群:对靛氰绿敏感患者。 检查前禁忌:无 检查时禁忌:(1)、检查前病人去称重,根据其重量给予一定剂量的靛氰绿。 (2)、检查其浓度时,要调好分光光度计计。 (3)、注射完了靛氰绿要等15分钟宇体内完全反应后便可抽取血。
-
概况 为了实现上述目标,石枫课题组基于对手性吲哚化学的理解(For a summary: Acc. Chem. Res. 2020, 53, 425),提出了基于3-芳基吲哚平台分子参与的催化不对称(2 + n)环化反应的策略,用于构建新型
-
药物中的杂质主要有两个来源,即药物生产过程中引入和药品贮藏过程中产生的。1.生产过程中引入的杂质生产过程中引入的杂质主要来源于以下几个方面:①所用原料不纯;②部分原料反应不完全;③反应中间产物或副产物在精制时未能完全除去;④生产过程
-
、4、5、7、8、分别编码5个进化上高度保守的结构域,P53基因5个高度保守区即第13~19、117~142、171~192、236~258、270~286编码区。P53基因转录成2.5KbmRNA,编码393个氨基酸蛋白,分子量为53
-
两种异构体主要用于有机合成,5,6.二羟基吲哚是黑素原的重要中间体, 黑色素是生物体内的酪氨酸经系列酶催化氧化反应形成。其中经过的一个最重要的中间体就是5,6-二羟基吲哚。5,6-二羟基吲哚是生物体内的物质,无毒、副作用。以对苯二胺
 2022-03-25来源: 2020年版中国药典
2022-03-25来源: 2020年版中国药典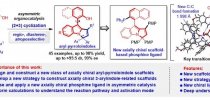 2022-02-08来源: X-MOL
2022-02-08来源: X-MOL

